OFFERTA SPECIALE
OFFERTA SPECIALE
Tutto il sito - Mese
6,99€ 1 € al mese x 12 mesi
oppure
1€ al mese per 6 mesi
Tutto il sito - Anno
79,99€ 9,99 € per 1 anno
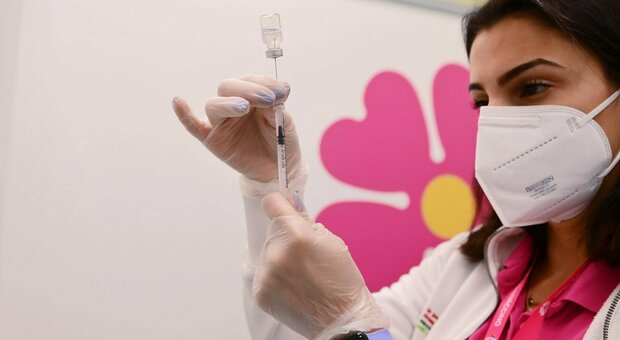
Moderna ha richiesto l'autorizzazione in Europa per la somministrazione del vaccino anti-Covid nei bambini dai 6 mesi ai 5 anni. La richiesta presentata all'Agenzia europea del farmaco Ema è per un'estensione dell'autorizzazione all'immissione in commercio condizionata (Cma), che includa un regime di due dosi da 25 microgrammi di Spikevax* in queste fasce d'età.
Attualmente il vaccino è autorizzato a partire dai 6 anni di età, ma secondo gli esperti della casa farmaceutica il siero è sicuro anche per i più piccoli: «Riteniamo - ha affermato Stéphane Bancel, Ceo di Moderna - che il vaccino mRNA-1273 sarà in grado di proteggere in sicurezza questi bambini contro Sars-CoV-2».
La casa farmaceutica già ieri aveva avanzato una richiesta analoga ieri presso la Fda (Food and Drug Administration) negli Stati Uniti richiedendo la possibilità di somminsitrare due dosi di vaccino a mRna da 25 microgrammi.
Vaccino bambini sotto ai 5 anni, gli studi: «Profilo di sicurezza favorevole»
A sostegno della propria tesi, Moderna ha presentato alle autorità degli Stati Uniti due studi di fase 2 e 3 KidCove tenuti nel mese di marzo, che dimostrano dopo due dosi di mRNA una «Robusta risposta anticorpale neutralizzante» nel gruppo di età compresa tra 6 mesi e meno di 6 anni e «un profilo di sicurezza favorevole» si legge in una nota diffusa dall'azienda statunitense. I titoli anticorpali nei sottogruppi di età da 6 mesi a 23 mesi e da 2 anni a 5 «hanno soddisfatto i criteri statistici di somiglianza con gli adulti nello studio COVE».
Un ulteriore studio è stato condotto sulla risposta dei vaccini alla variante Omicron nei più piccoli. Durante l'ondata omicron sono stati analizzati i dati dei bambini confermati positivi con test molecolare che erano stati vaccinati: «L'efficacia del vaccino è rimasta significativa al 51% per i bebè under 2 e al 37% da 2 a 5 anni. Queste stime di efficacia sono simili alle stime di efficacia del vaccino contro Omicron negli adulti», evidenzia Moderna.
Leggi l'articolo completo su
Il Messaggero